Муковисцидоз (кистозный фиброз) – наследственное заболевание, которое вызывается мутацией гена трансмембранного регулятора муковисцидоза. Проявляется в системном поражении желез внешней секреции и сопровождается тяжелыми нарушениями функций желудочно-кишечного тракта, органов дыхания и ряда других органов и систем.
| МКБ-10 | E84 |
|---|---|
| МКБ-9 | 277.0 |
| DiseasesDB | 3347 |
| MedlinePlus | 000107 |
| eMedicine | ped/535 |
| OMIM | 219700 |
| MeSH | D003550 |
Общие сведения
Первое упоминание заболевания относится к 1905 г.- в это время австрийским врачом иммунологом Карлом Ландштейнером при описании кистозных изменений поджелудочной железы при мекониальной непроходимости у двух детей высказывается мысль о взаимосвязи этих явлений.
Заболевание подробно описала, выделила как самостоятельную нозологическую единицу и доказала ее наследственный характер американский патологоанатом Дороти Андерсон в 1938 г.
Название “муковисцидоз” (от лат. Mucus – слизь, viscus – вязкий) в 1946 году предложила использовать Сидни Фарбер, американский педиатр.
Частота распространения широко варьирует в различных этнических группах. Наиболее часто муковисцидоз встречается в Европе (в среднем 1:2000 — 1:2500), но заболевание зарегистрировано у представителей всех рас. Частота муковисцидоза у коренного населения Африки и Японии составляет 1:100000. В России в среднем распространенность заболевания составляет 1:10000.
Пол ребенка не влияет на частоту заболевания.
Наследование происходит по аутосомно-рецессивному типу. У носителей одного дефектного гена (аллели) муковисцидоз не проявляется. Если оба родителя – носители мутировавшего гена, риск рождения больного муковисцидозом ребенка составляет 25 %.
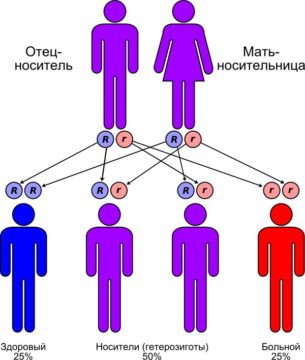
В Европе каждый 30-й житель – носитель дефектного гена.
Формы
В зависимости от места локализации поражения муковисцидоз разделяют на:
- Легочную (респираторную) форму заболевания (15-20% от всех случаев). Проявляется признаками поражения дыхательного аппарата вследствие скопления большого количества вязкой трудноотделяемой мокроты в мелких и средних бронхах.
- Кишечную форму (5% от всех случаев). Проявляется в нарушении переваривания и усвоения пищи, повышенной жажде.
- Смешанную форму (легочно-кишечную, на долю которой приходится 75-80% случаев). Поскольку данная форма сочетает клинические признаки респираторной и кишечной форм муковисцидоза, ей свойственно более тяжелое течение заболевания и вариативность его проявлений.
Отдельно выделяется мекониевая непроходимость, при которой в результате пониженной активности ферментов поджелудочной железы и недостаточной выработке жидкой части секрета клетками кишечного эпителия прилипший к стенке кишечника меконий (первородный кал) закупоривает просвет и вызывает кишечную непроходимость.
Встречаются также обусловленные разновидностями мутаций гена CFTR:
- атипичные формы, которые проявляются в изолированных поражениях желез внутренней секреции (цирротическая, отечно – анемическая);
- стертые формы, выявляющиеся обычно случайно, поскольку протекают аналогично другим заболеваниям и диагностируются как цирроз печени, синусит, хронические обструктивные болезни легких, рецидивирующий бронхит и мужское бесплодие.
Причины развития
Муковисцидоз вызван мутациями расположенного на длинном плече 7-й хромосомы гена CFTR. Данный ген встречается у многих животных (коровы, мыши и др.). Он содержит около 250 000 пар нуклеотидов и состоит из 27 экзонов.
Кодируемый данным геном и отвечающий за транспорт ионов хлора и натрия через клеточную мембрану белок располагается в основном в клетках эпителия дыхательных путей, кишечника, поджелудочной железы, слюнных и потовых желез.
Сам ген CFTR был выявлен в 1989 году, и уже к настоящему времени обнаружено около 2000 вариантов его мутаций и 200 полиморфизмов (вариабельных участков в последовательности ДНК).
У представителей европейской расы наиболее часто встречается мутация F508del. Максимальное количество случаев данной мутации зарегистрировано в Великобритании и Дании (85%), а минимальное – среди населения Ближнего Востока (до 30%).
Некоторые мутации часто встречаются у представителей определенных этнических групп:
- в Германии – мутация 2143delT;
- в Исландии – мутация Y122X;
- у евреев-ашкенази – W1282X.
В России 52% мутаций, вызывающих муковисцидоз, приходится на мутацию F508del, 6,3 % – на мутацию CFTRdele2,3(21kb), 2,7% – на мутацию W1282X. Встречаются также такие типы мутации, как N1303K, 2143delT, G542X, 2184insA, 3849+10kbC-T, R334W и S1196X, но их частота не превышает 2,4%.
Тяжесть заболевания зависит от типа мутации, ее локализации в определенном регионе и специфики ее воздействия на функцию и структуру кодируемого белка. Тяжелым течением болезни и наличием сопутствующих осложнений и внешнесекреторной недостаточности поджелудочной железы отличаются мутации F508del, CFTRdele2,3(21kb), W1282X, N1303K и G542X.
К тяжелым случаям муковисцидоза относится и заболевание, вызванное мутацией DF508, G551D, R553X, 1677delTA, 621+1G-A и 1717-1G-A.
В более легкой форме протекает муковисцидоз, вызванный мутациями R117H, 3849+10kbC-T, R 374P, T338I, G551S.
При мутациях G85E, R334W и 5T тяжесть течения заболевания варьируется.
К мутациям, блокирующим синтез белка, относятся мутации G542Х, W1282Х, R553X, 621+1G-T, 2143delT, 1677delTA.
Мутации, вызывающие нарушение посттрансляционной модификации белков и их превращение в зрелую РНК (процессинг), включают мутации DelF508, dI507, S549I, S549R, N1303K.
Выявлены также мутации:
- нарушающие регуляцию белка (G551D, G1244E, S1255P);
- снижающие проводимость ионов хлора (R334W, R347P, R117H);
- снижающие уровень белка или нормальной РНК (3849+10kbC-T, A455E, 5T, 1811+1,6kbA-G).
В результате мутации строение и функции белка CFTR нарушаются, поэтому секрет эндокринных желез (пот, слизь, слюна) становится густым и вязким. Содержание белка и электролитов в секрете повышается, концентрация натрия, кальция и хлора увеличивается, а эвакуация секрета из выводных протоков значительно затрудняется.
В результате задержки густого секрета протоки расширяются и формируются мелкие кисты.
Постоянный застой слизи (мукостаз) вызывает атрофию железистой ткани и ее постепенное замещение соединительной тканью (фиброз), развиваются ранние склеротические изменения в органах. При вторичном инфицировании заболевание осложняется гнойным воспалением.
Патогенез
Муковисцидоз вызывается неспособностью дефектного белка полноценно выполнять свои функции.
В результате нарушений функций белка в клетках постепенно накапливается повышенное количество ионов хлора и меняется электрический потенциал клетки.
Смена электрического потенциала вызывает поступление в клетку ионов натрия. Избыток ионов натрия провоцирует усиленное всасывание воды из околоклеточного пространства, а недостаток воды в околоклеточном пространстве обуславливает сгущение секрета экзокринных желез.
При затрудненной эвакуации густого секрета в первую очередь поражаются бронхолегочная и пищеварительная системы.
Нарушение проходимости мелких бронхов и бронхиол приводит к развитию хронического воспаления и разрушению соединительнотканного каркаса. Дальнейшее развитие заболевания сопровождается формированием мешотчатых, цилиндрических и «каплевидных» бронхоэктазов (расширение бронхов) и эмфизематозных (раздутых) участков легкого.
Бронхоэктазы с одинаковой частотой наблюдаются в верхних и нижних долях легких. В большинстве случаев не выявляются у детей на первом месяце жизни, но уже к 6-му месяцу наблюдаются в 58% случаев, а после полугода – в 100 % случаев. В этом возрасте в бронхах обнаруживаются различные изменения (катаральный или диффузный бронхит, эндобронхит).
Бронхиальный эпителий в некоторых местах слущивается, наблюдаются очаги гиперплазии бокаловидных клеток и плоскоклеточной метаплазии.
При полной закупорке мокротой бронхов образуются зоны спадения доли легкого (ателектаз), а также склеротические изменения легочной ткани (развивается диффузный пневмосклероз). Во всех слоях стенок бронха присутствует инфильтрация лимфоцитами, нейтрофилами и плазматическими клетками.
Устья слизистых бронхиальных желез расширяются, в них выявляются гнойные пробки, а в просветах бронхоэктазов присутствует большое количество фибрина, распадающиеся лейкоциты, некротизированный бронхиальный эпителий и колонии кокков. Мышечный слой атрофирован, а стенки бронхоэктазов истончены.
В случае присоединения бактериальной инфекции на фоне нарушения иммунитета начинается абсцедирование и развиваются деструктивные изменения (синегнойная палочка высевается в 30 % случаев). При скоплении пенистых клеток и эозинофильных масс с включением липидов благодаря нарушению гомеостаза происходит развитие вторичного липопротеоноза.
К 24 годам пневмония выявляется в 82 % случаев.
Продолжительность жизни при муковисцидозе зависит от состояния бронхолегочной системы, поскольку у больного благодаря прогрессирующему изменению сосудов малого круга кровообращения постепенно снижается количество кислорода в крови и увеличиваются и расширяются правые отделы сердца (развивается «легочное сердце»).
Наблюдаются и другие изменения в области сердца. У больных выявляют:
- миокардиодистрофию (нарушение метаболизма сердечной мышцы) с интерстициальным склерозом;
- очаги миксоматоза миокарда;
- истончение мышечных волокон;
- отсутствие местами поперечной исчерченности;
- склеротические очаги (интерстициальный склероз) в области сосудов;
- умеренное набухание эндотелия сосудов;
- кардиодистрофию, выраженную в разной степени.
Возможен клапанный и пристеночный эндокардит.
При сгущении секрета поджелудочной железы закупорка ее протоков часто происходит еще в период внутриутробного развития. В таких случаях вырабатываемые этой железой в нормальном количестве панкреатические ферменты не способны достичь двенадцатиперстной кишки, поэтому они накапливаются и вызывают распад ткани в самой железе. К концу первого месяца жизни поджелудочная железа таких больных является скоплением фиброзной ткани и кист.
Киста возникает в результате расширения междольковых и внутридольковых проток и уплощения и атрофирования эпителия. Внутри долек и между ними наблюдается разрастание соединительной ткани и ее инфильтрация нейтрофилами и лимфогистиоцитарными элементами. Развивается также гиперплазия островкового аппарата, атрофирование паренхимы железы и жировое перерождение ткани.
Эпителий кишечника становится уплощенным и включает повышенное количество бокаловидных клеток, а в криптах присутствует скопление слизи. Слизистая оболочка инфильтрирована лимфоидными клетками с включением нейтрофилов.
Мутации, которые сопровождаются снижением проводимость ионов хлора или уровня белка или нормальной РНК, вызывают медленное развитие хронического панкреатита при относительной сохранности функции поджелудочной железы на протяжении длительного времени.
Муковисцидоз у новорожденных в 20% случаев приводит к закупорке густым меконием дистальных отделов тонкой кишки.
В отдельных случаях заболевание сопровождается длительной неонатальной желтухой, которая вызывается вязкостью желчи и повышенным образованием билирубина.
Практически у всех больных наблюдается уплотнение соединительной ткани и рубцовые изменения в печени (фиброз). В 5-10 % случаев патология прогрессирует и вызывает билиарный цирроз и портальную гипертензию.
Также в печени выявляют наличие:
- очаговой или диффузной жировой и белковой дистрофии клеток;
- застоя желчи в междольковых желчных протоках;
- лимфогистиоцитарных инфильтратов в междольковых прослойках.
Муковисцидоз сопровождается аномалией функции потовых желез – концентрация натрия и хлора в секрете повышена, и количество соли превышает норму приблизительно в 5 раз. Эта патология наблюдается в течение всей жизни больного, поэтому жаркий климат людям, страдающим муковисцидозом, противопоказан (повышается риск получить тепловой удар, возможны судороги вследствие развития метаболического алкалоза).
Симптомы
Муковисцидоз в большинстве случаев проявляется до годовалого возраста.
В 10% случаев симптомы заболевания (мекониевая непроходимость кишечника или мекониальный илеус) обнаруживаются при ультразвуковом исследовании еще в период внутриутробного развития во 2-3 триместре.
У части детей кишечная непроходимость обнаруживается в первые дни жизни. Признаками мекониального илеуса являются:
- отсутствие физиологического выделения мекония;
- вздутие живота;
- беспокойство;
- срыгивания;
- рвота, при которой в рвотных массах обнаруживается присутствие желчи.
На протяжении двух дней состояние ребенка ухудшается – появляется бледность и сухость кожных покровов, снижается тургор тканей, появляется вялость и адинамия. Развивается обезвоживание и нарастает интоксикация. В некоторых случаях возможно развитие осложнения (перфорация кишечника и перитонит).
Кишечный муковисцидоз проявляется в большинстве случаев после введения прикорма или искусственного вскармливания благодаря недостаточности панкреатических ферментов. Симптомами данной формы заболевания являются:
- вздутие живота;
- частые дефекации
- значительно увеличенное выделение кала;
- зловонность и светлый цвет кала, присутствие в нем значительного количества жира.
Возможно выпадение прямой кишки при высаживании на горшок (наблюдается у 10-20% больных).
Часто присутствует ощущение сухости во рту, возникающее из-за вязкости слюны, поэтому прием сухой пищи затруднен, и в процессе еды больные вынуждены в большом количестве употреблять жидкость.
Аппетит на начальных этапах может быть повышен или соответствовать норме, но благодаря нарушениям пищеварения впоследствии развивается гиповитаминоз и гипотрофия. В процессе развития заболевания присоединяются признаки цирроза и холестатического гепатита (повышенная утомляемость, похудание, желтуха, потемнение мочи, нарушения поведения и сознания, боли в животе и др.).
Муковисцидоз легких благодаря гиперпродукции в бронхолегочной системе вязкого секрета вызывает обструктивный синдром, который проявляется:
- удлинением выдоха;
- появлением свистящего шумного дыхания;
- приступами удушья;
- участием в дыхательном акте вспомогательной мускулатуры.
Возможен малопродуктивный кашель.
Инфекционно-воспалительный процесс носит хронический рецидивирующий характер. Наблюдаются осложнения в виде гнойно-обструктивного бронхита и тяжелых пневмоний со склонностью к абсцедированию.
Симптомами легочной формы заболевания являются:
- бледно-землистый оттенок кожи;
- вызванная недостаточным кровоснабжением синюшная окраска кожи;
- наличие одышки в состоянии покоя;
- бочкообразная деформация грудной клетки;
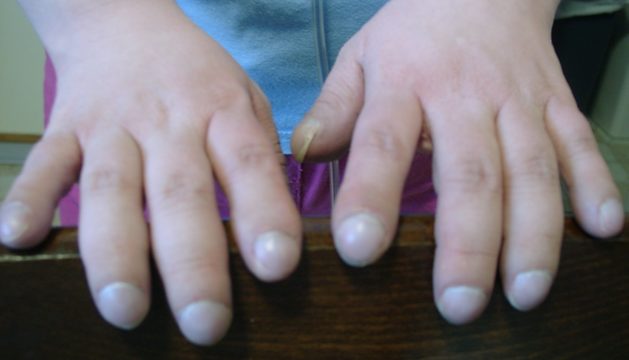
- деформация пальцев рук (концевые фаланги напоминают барабанные палочки) и ногтей (напоминают часовые стекла);
- пониженная двигательная активность;
- снижение аппетита;
- низкая масса тела.
Бронхиальное содержимое обычно включает синегнойную палочку, золотистый стафилококк и гемофильную палочку. Флора может проявлять устойчивость к антибиотикам.
Легочная форма оканчивается летальным исходом в связи с тяжелой дыхательной и сердечной недостаточностью.
Признаки муковисцидоза при смешанной форме включают симптомы кишечной и легочной форм.
Стертые формы заболевания диагностируются обычно в зрелом возрасте, поскольку особые разновидности мутаций в гене CFTR вызывают более легкое течение болезни, а ее симптомы совпадают с симптомами синусита, рецидивирующего бронхита, хронических обструктивных болезней легких, цирроза печени или мужского бесплодия.
Муковисцидоз у взрослых часто вызывает бесплодие. У 97 % мужчин, больных муковисцидозом, выявляется врожденное отсутствие, атрофия или обструкция семенного канатика, а у большинства страдающих муковисцидозом женщин наблюдается снижение фертильности из-за повышенной вязкости слизи цервикального канала. При этом у части женщин детородная функция сохраняется. Также иногда встречаются мутации гена CFTR у мужчин, не имеющих признаков муковисцидоза (следствием мутации в 80% таких случаев является аплазия семявыносящего протока).
На умственном развитии муковисцидоз не сказывается. Тяжесть течения заболевания и его прогноз зависят от сроков манифестации болезни – чем позже проявились первые симптомы, тем легче протекает заболевание и тем благоприятнее прогноз.
Поскольку муковисцидоз благодаря большому количеству вариантов мутаций отличается полиморфизмом клинических проявлений, тяжесть заболевания оценивают по состоянию бронхолегочной системы. Выделяются 4 стадии:
- 1-я, для которой характерны непостоянные функциональные изменения, сухой кашель без отделения мокроты, незначительная или умеренная одышка при физических нагрузках. Длительность первой стадии может достигать 10 лет.
- 2-я стадия, для которой свойственно развитие хронического бронхита, наличие кашля, сопровождающегося отделением мокроты, умеренная в покое и усиливающаяся при напряжении одышка, деформация концевых фаланг пальцев. При выслушивании выявляется наличие жесткого дыхания с влажными, «трескучими» хрипами. Данная стадия длится от 2 до 15 лет.
- 3-я стадия, на которой возникают осложнения и прогрессирует патологический процесс в бронхолегочной системе. Происходит формирование бронхоэктазов, зон диффузного пневмофиброза и ограниченного пневмосклероза, кист. Наблюдается сердечная недостаточность (правожелудочковый тип) и выраженная дыхательная недостаточность. Продолжительность стадии составляет от 3 до 5 лет.
- 4-я стадия, для которой характерна тяжелая кардио-респираторная недостаточность, оканчивающаяся летальным исходом в течение нескольких месяцев.
Диагностика
Диагноз «муковисцидоз» основан на:
- опорно-диагностических признаках, включающих семейный анамнез, срок манифестации заболевания, его прогрессирующее течение, наличие характерного поражения пищеварительной и бронхолегочной системы, проблемы с деторождением (наличие бесплодия или сниженная фертильность);
- данных основных лабораторных методов диагностики;
- ДНК-диагностике.
К лабораторным методам, позволяющим выявить муковисцидоз у детей, относятся:
- ИРТ (тест на фермент поджелудочной железы иммунореактивный трипсин), который информативен у новорожденных только в течение первого месяца жизни. Благодаря данному тесту определяется уровень содержания этого фермента в крови. У новорожденных при муковисцидозе уровень иммунореактивного трипсина повышен в 5-10 раз. Тест может дать ложноположительные результаты при наличии у ребенка глубокой недоношенности, синдрома Эдвардса, множественных врожденных пороков развития (МВПР) или асфиксии в родах.
- Потовый тест, который проводится по методу Гибсона-Кука. Метод заключается во введении в кожу при помощи слабого электрического тока ионофореза пилокарпина (препарат, стимулирующий потовые железы). Пот в количестве минимум 100 гр. собирается, взвешивается, после чего определяется концентрация в нем ионов натрия и хлора. При наличии потовых анализаторов использование метода упрощается. В норме концентрация в секрете потовых желез натрия и хлора не превышает 40 ммоль/л. При наличии у ребенка адреногенитального синдрома, ВИЧ-инфекции, гипогаммаглобулинемии, гипотиреоза, семейного гипопаратиреоза, гликогеноза 2-го типа, дефицита глюкозо-6-фосфатазы, синдромов Мориака или Клайнфельтера, мукополисахаридоза, нефрогенного несахарного диабета, псевдогипоальдостеронизма, фруктозидоза или цеалкии тест может быть ложноположительным, а при лечении некоторыми антибиотиками – ложноотрицательным.
- NPD-тест, который заключается в измерении трансэпителиальной разности назальных электрических потенциалов. Норма разности потенциалов – от -5 mV до -40 mV.
Наиболее точно диагностировать муковисцидоз помогает ДНК-диагностика. Для исследования обычно используются:
- Жидкая кровь, которая в количестве около 1 мл помещается в пробирку с антикоагулянтом (гепарин использовать недопустимо).
- Высушенное при комнатной температуре пятно крови диаметром около 2 см, расположенное на марле или бумажном фильтре. Образцы можно исследовать в течение нескольких лет.
- Гистологические образцы, которые используются для проведения анализа у умершего.
Возможно использование:
- Прямой диагностики, позволяющей выявить конкретную мутацию в определенном гене.
- Косвенной диагностики, при которой анализируется наследование сцепленных с геном заболевания генетических маркеров. Возможно только при наличии в семье больного муковисцидозом ребенка, поскольку установить молекулярный маркер возможно только по анализу его ДНК.
В большинстве случаев для исследования используется метод ПЦР (полимеразной цепной реакции). Самые распространенные типы мутаций в гене CFTR выявляются при помощи специально разработанных диагностикумов, позволяющих одновременно выявлять несколько мутаций.
Диагностировать муковисцидоз помогают также инструментальные методы обследования:
- рентгенография, позволяющая выявить наличие характерных изменений в легких (инфильтрацию, эмфизему, расширение корней легких, деформацию легочного рисунка);
- бронхография, которая помогает выявить снижение числа разветвлений бронхов, обрывы их заполнения, наличие цилиндрических или смешанных бронхоэктазов;
- бронхоскопия, при помощи которой можно выявить наличие высоковязкого слизисто-гнойного секрета и диффузного гнойного эндобронхита;
- спирография, позволяющая обнаружить наличие нарушений функций внешнего дыхания по обструктивно-рестриктивному типу;
- копрограмма, которая позволяет выявить наличие большого количества неперевариваемого жира.
Муковисцидоз также диагностируется при помощи исследования дуоденального содержимого, которое помогает выявить в дуоденальном соке снижение количества ферментов или их отсутствие.
Экзокринную функцию поджелудочной железы оценивают при помощи теста на наличие в кале панкреатической эластазы 1(E1). Муковисцидоз проявляется значительным снижением содержания эластазы 1 (умеренное снижение свидетельствует о наличии хронического панкреатита, опухоли поджелудочной железы, холелитиаза или диабета).
Муковисцидоз можно также выявить при помощи пренатальной диагностики. Образцы ДНК выделяются на 9-14 неделе беременности из биоптата ворсин хориона. При более поздних сроках обращения семьи для диагностики используют амниотическую жидкость (16-21 недели) или полученную путем кордоцентеза кровь плода (после 21 недели).
Пренатальная диагностика проводится при наличии мутаций у обоих родителей или при гомозиготности имеющегося в семье больного ребенка. Рекомендуется пренатальная диагностика и при наличии мутаций только у одного родителя. Выявленная у плода аналогичная мутация требует дифференциации между гомозиготной инактивацией гена и бессимптомным гетерозиготным носительством. Для дифференциальной диагностики на 17-18 неделе проводится биохимическое исследование амниотической жидкости на активность аминопептидазы, гамма-глютамилтранспептидазы и кишечной формы щелочной фосфотазы (муковисцидоз отличается снижением количества данных кишечных ферментов).
Если мутации гена CFTR не удается выявить, а больной муковисцидозом ребенок уже умер, обследование плода проводится при помощи биохимических методов, так как пренатальная молекулярно-генетическая диагностика считается в таком случае неинформативной.
Лечение
Муковисцидоз у детей предпочтительнее лечить в специализированных центрах, поскольку больные нуждаются в комплексной медицинской помощи, включающей помощь врачей, диетологов, психологов, кинезитерапевтов и социальных работников.
Поскольку муковисцидоз как генетическое заболевание неизлечим, целью терапии является поддержание образа жизни, максимально совпадающего с образом жизни здоровых детей. Больные муковисцидозом нуждаются в:
- обеспечении адекватного, богатого белками и без ограничения в количестве жиров, диетического питания;
- контроле над респираторными инфекциями;
- ферментотерапии с использованием препаратов поджелудочной железы;
- муколитической терапии, направленной на торможение образования бронхиального секрета и его разжижение;
- антимикробной и противовоспалительной терапии;
- витаминотерапии;
- своевременном лечении осложнений.
Для лечения синдрома мальабсорбции (потери поступающих в пищеварительный тракт питательных веществ), обусловленного недостаточностью ферментов поджелудочной железы, применяют панкреатические ферменты в виде микрогранул (Креон 10000, Креон 25000). Препараты применяются во время еды, а доза подбирается индивидуально.
Поскольку недостаточность поджелудочной железы при муковисцидозе полностью не корректируется, о достаточности дозы свидетельствует нормализация характера стула и его частоты, а также лабораторные данные (в копрограмме не обнаруживается стеаторея и креаторея, в липидограмме нормализуется концентрация триглицеридов).
Респираторный муковисцидоз требует применения:
- Муколитической терапии, которая включает использование тиолов, способных эффективно разжижать бронхиальный секрет. Применяется перорально, внутривенно или ингаляционно, N-ацетилцистеин, обладающий не только муколитическим, но и антиоксидантным эффектом. Эффективны ингаляции через маску с использованием рекомбинантной человеческой ДНК-азы (Пульмозим, Дорназа альфа). Хорошо разжижают и эвакуируют мокроту ингаляции с гипертоническим раствором хлорида натрия (7%).
- Кинезитерапии. Для очищения от патологического секрета бронхиального дерева и предотвращения инфекционного поражения легких используется постуральный дренаж, аутогенный дренаж, перкуссия и клопфмассаж (заключается в вибрации грудной клетки). Применяется также активный цикл дыхания, ПЕП-маски и дыхательные упражнения с использованием флаттера.
- Антибиотикотерапии. Препарат выбирается в зависимости от вида выделенных из бронхиального секрета микроорганизмов и результатами лабораторных тестов на чувствительность к антибиотикам . Поскольку применение различных схем антибиотикотерапии предупреждает или задерживает развитие хронической инфекции бронхолегочной системы, антибиотики применяются длительное время и могут назначаться в профилактических целях.
Для лечения синегнойной инфекции антибиотики обычно вводятся внутривенно.
Критерием для отмены антибиотикотерапии является возврат основных симптомов обострения к исходному для данного пациента состоянию.
Муковисцидоз является противопоказанием к применению противокашлевых препаратов.
Эффективное лечение прогрессирующего поражения печени при муковисцидозе в настоящее время не разработано. Обычно больным при начальных признаках поражения печени назначается урсодеоксихолевая кислота в дозе не менее 15-30 мг/кг/сут.
Поскольку на повреждении легочной ткани сказывается чрезмерный иммунный ответ организма, в качестве противовоспалительной терапии используются макролиды, нестероидные противовоспалительные средства и системные и местные глюкокортикоиды.
При муковисцидозе рекомендуются занятия некоторыми видами спорта (волейбол, бег, плаванье и др.).
Муковисцидоз – заболевание, при котором больной нуждается в регулярных детальных обследованиях, включающих исследование функции внешнего дыхания, копрограмму, антропометрию, общие анализы мочи и крови. Раз в год проводят рентгенографию грудной клетки, ЭхоКГ и УЗИ органов брюшной полости, определяют костный возраст, делают иммунологический и биохимический анализы крови.
