Фенилкетонурия (ФКУ) – редкое генетическое заболевание, связанное с нарушением обмена фенилаланина (протеиногенной аминокислоты), поступающего в организм в составе белковой пищи. Вызывает накопление в организме фенилаланина и его токсических производных, что приводит к поражению ЦНС.
| МКБ-10 | E70.0 |
|---|---|
| МКБ-9 | 270.1 |
| DiseasesDB | 9987 |
| MedlinePlus | 001166 |
| eMedicine | ped/1787 derm/712 |
| MeSH | D010661 |
| OMIM | 261600 261630 |
Общие сведения
Фенилкетонурия известна с 1934 года, но вследствие отсутствия качественной диагностики заболевание выявлялось только на той стадии, когда в результате токсичного воздействия на головной мозг нарушения умственного развития становятся необратимыми. Именно поэтому заболевание получило второе название – фенилпировиноградная олигофрения.
По статистике нарушение обмена фенилаланина чаще наблюдается у девочек. Распространено больше в Турции, северных странах Европы (исключение – Финляндия), и крайне редко встречается у представителей негроидной расы. Поскольку фенилкетонурия относится к заболеваниям, при которых дефективный ген наследуется от обоих родителей, браки между родственниками увеличивают вероятность рождения детей, страдающих этим заболеванием.
Впервые имевшее успех лечение провели в детском госпитале Бирмингема (Англия) в 50-х гг. XX века, но по-настоящему эффективным этот метод лечения стал после внедрения в начале 60-х гг. ранней диагностики.
Виды
Фенилаланин под воздействием ферментов в организме преобразуется в тирозин – аминокислоту, которая выводится из организма. В зависимости от дефекта гена, блокирующего определенный фермент, выделяют:
- Фенилкетонурию I-го типа (классическую или тяжелую). Вызывается генной мутацией, нарушающей выработку печеночного фермента фенилаланингидроксилазы и преобразование фенилаланина в тирозин.
- Фенилкетонурию II-го типа (атипичную). Характеризуется генным дефектом, вызывающим недостаток дигидробиоптерин-редуктазы. Благодаря этому фактору нарушается восстановление активности органического соединения, необходимого для преобразования фенилаланина. Также наблюдается пониженное содержание в спинномозговой жидкости и в сыворотке крови витамина В9, необходимого для утилизации аминокислот.
- Фенилкетонурию III-го типа (атипичную). Провоцируется нехваткой катализатора, необходимого для синтеза тетрагидробиоптерина (нужен для преобразования фенилаланина в тирозин).
- Примаптеринурию – атипичную форму, которая наблюдается при легкой форме гиперфенилаланинемии. Ферментный дефект этого вида ФКУ в настоящее время не выяснен, но данная форма заболевания характеризуется значительным количеством примаптерина и его производных в моче, а количество нейромедиаторных метаболитов в спинномозговой жидкости не отклоняется от нормы.
Выделяется также материнская фенилкетонурия, наблюдающаяся у потомства женщин, больных ФКУ и не соблюдающих специализированную диету. Патогенез данной формы заболевания до конца не изучен, но отмечается, что без постоянного контроля за уровнем фенилаланина у новорожденных обнаруживается ряд патологических изменений:
- недостаточный вес мозга;
- увеличенные в размерах желудочки головного мозга (вентрикуломегалия);
- гипоплазия (недоразвитие) белого вещества и задержка миелинизации.
Фенилкетонурия данного типа вызывает хроническую интоксикацию плода и приводит к умственной отсталости ребенка.
Причины развития
Фенилпировиноградная олигофрения возникает при наличии патологического гена у матери и отца. Тип наследования – аутосомно-рецессивный, то есть не зависит от пола ребенка. Вероятность развития заболевания у новорожденных, родители которых являются носителями дефектного гена, составляет 25%.
Патогенез
В результате вызванного генным дефектом нарушения обмена фенилаланина и его последующего превращения в тирозин в организме накапливаются токсические производные этой аминокислоты (фенилпировиноградная, фенилмолочная и фенилуксусная кислоты), в норме встречающиеся в минимальном количестве. Образуются также не встречающиеся в норме ортофенилацетат и фенилэтиламин, нарушающие липидный обмен в головном мозге, что служит причиной прогрессирующего снижения интеллекта.
Факторами, влияющими на развитие патологии, являются:
- нарушения аминокислотного обмена;
- нарушения миелинизации;
- нарушение синтеза протеолипидных белков,
- пониженный уровень нейротрансмиттеров (адреналина, серотонина и др.).
Симптомы
Сразу после рождения у детей с ФКУ I симптомы болезни не наблюдаются, хотя обычно имеется специфический ряд внешних признаков:
- Суховатая кожа белого оттенка (почти полностью отсутствует пигментация).
- Голубые глаза.
- Волосы светлых оттенков.
В возрасте 2-х – 6-ти месяцев проявляются первые признаки заболевания:
- вялость (не делает попыток перевернуться, сесть);
- пассивное восприятие окружающего (не реагирует на мать, не отвечает улыбкой);
- повышенная раздражительность;
- задержка психомоторного развития.
Возможна интенсивная частая рвота и беспокойство, приступы судорог.
Если заболевание своевременно не выявлено и в рацион ребенка вводят белковую пищу, симптоматика начинает нарастать. У таких детей поздно прорезываются зубы, а череп несколько уменьшен в размерах. Сидеть и ходить начинают позже сверстников, мимика невыразительна, в год не способны выразить голосом эмоции, речь взрослых не понимают. Возможна задержка роста.
Поскольку фенилаланин в организме не преобразуется, он выводится с потом и мочой, поэтому от больных исходит затхлый или «мышиный» запах.
Фенилкетонурия у детей проявляется также в своеобразных позах и походке, так как мышечный тонус у таких больных повышен. В положении стоя ноги у ребенка широко расставлены и согнуты в коленях и тазобедренных суставах, голова и плечи опущены. Походка качающаяся, шаги мелкие. Сидят они в положении портного (поджимают и скрещивают ноги).
Фенилпировиноградная олигофрения после трехлетнего возраста проявляется в:
- повышенной возбудимости и утомляемости;
- нарушениях поведения;
- психотических расстройствах;
- умственной отсталости.
Часто наблюдается экзема, склеродермия и дерматит.
При отсутствии лечения состояние больных ухудшается. Своевременно поставленный диагноз и лечение позволяют предотвратить нарушения развития ребенка.
Диагностика
Диагностировать заболевание можно:
- полуколичественным тестом, который позволяет определить приблизительное количество фенилаланина в крови;
- количественным определением при помощи реагентов, выявляющих количество фенилаланина в высохших кровяных пятнах.
Для этого обследования в роддоме в день выписки или на 5-й день жизни у всех детей после кормления берется кровь из пятки.
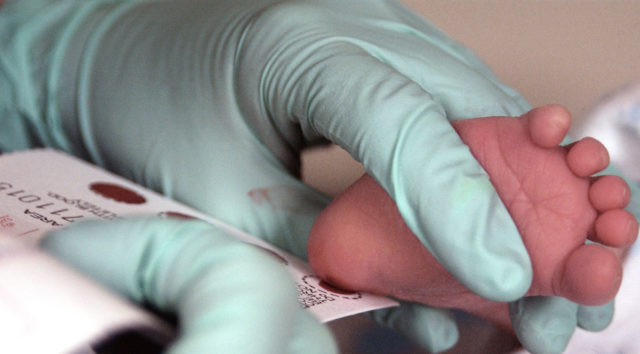
Диагностика включает и исследование мочи (проба Феллинга), но оно информативно только после 10-12 дня жизни ребенка. Фенилпировиноградная кислота проявляется сине-зеленой окраской в моче при добавлении в мочу хлорида железа.
Можно также определить активность фермента фенилаланингидроксилазы в материале, полученном методом биопсии, и обнаружить мутации в гене.
Используются также такие методы, как:
- тест Гатри, основанный на добавлении крови в бактериальную культуру, быстро растущую в фенилаланиновой среде;
- тонкослойная хроматография аминокислот, содержащихся в сыворотке крови;
- флуориметрия, позволяющая выявить микродозы фенилаланина благодаря облучению ультрафиолетом.
Фенилкетонурия 2 и 3 типа диагностируется при помощи исследования биоптеринов мочи, перорального нагрузочного теста с тетрагидробиоптерином, энзиматических исследований.
Выявлять фенилкетонурию можно и с помощью генетического анализа, который обычно проводят при наличии членов семьи с данным диагнозом.
Лечение
При своевременно поставленном диагнозе лечение фенилкетонурии заключается в специализированной диете, ограничивающей поступление пищи, содержащей фенилаланин. Так как все естественные источники белка содержат около 4% фенилаланина, они заменяются содержащими другие аминокислоты синтетическими продуктами. Наиболее эффективна диета, назначенная до 8-й недели жизни.
Грудным детям назначаются полностью очищенные от лактозы смеси на основе гидролизата молочного белка. Материнское молоко допустимо в ограниченном количестве.
Хотя раньше врачи рекомендовали соблюдать диету только до окончания развития головного мозга (20 лет), повышение уровня фенилаланина после прекращения диеты у многих людей вызывает психиатрические проблемы. Фенилкетонурия у взрослых проявляется недостаточностью мотивации, бессонницей и деконцентрацией, импульсивностью и т.д., поэтому диету рекомендуется соблюдать пожизненно.
Диетические ограничения, введенные после 2-х лет, способны только снизить выраженность симптомов.
Для лечения применяются также препараты:
- относящиеся к ноотропной группе (ноотропил и др.). Они стимулируют умственную деятельность и активизируют когнитивные функции;
- содержащие витамины, аминокислоты и белки (“Афенилак” и т.д.).
Атипичные формы фенилкетонурии не поддаются диетотерапии и требуют дополнительного медикаментозного лечения, которое включает:
- Дигидробиоптерин, компенсирующий недостаток фолиевой кислоты;
- Леводол, действующий на ЦНС.
Пациентам, нуждающимся в дополнительной коррекции нейромедиаторов, назначают “Мадопар” или “Наком”.
Взрослым назначаются растительные препараты, содержащие фенилаланингидроксилазу.
Профилактика
Поскольку фенилкетонурия – генетическое заболевание, полностью предотвратить его развитие нельзя. Профилактические меры направлены на предотвращение необратимых тяжелых нарушений развития мозга путем своевременной диагностики и диетотерапии.
Семьям, в которых уже были случаи данного заболевания, рекомендуется проведение генетического анализа, способного предсказать возможное развитие фенилкетонурии у ребенка.
Женщинам с ФКУ рекомендуется до зачатия и во время беременности придерживаться диеты с низким содержанием фенилаланина.

